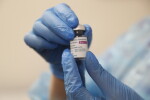
Агенцията за регулиране на лекарствата и здравните продукти на Великобритания (MHRA) и Европейската агенция по лекарствата (EMA) завършиха своята оценка на изключително редки събития на тромбози с ниски тромбоцити от над 34 милиона души, ваксинирани с ваксината COVID-19 на „АстраЗенека“ във Великобритания и ЕС.
Компанията вече работи, за да разбере отделните случаи, епидемиологията и възможните механизми, които биха могли да обяснят тези изключително редки събития, се посочва в официална позиция на „АстраЗенека“, изпратена до медиите.
„Регулаторите поискаха актуализация на информацията за ваксината във Великобритания и ЕС. Нито една от агенциите не е идентифицирала никакви рискови фактори, като възраст или пол, или определена причина за тези изключително редки събития. Те обаче стигнаха до мнението, че тези събития имат възможна връзка с ваксината и поискаха те да бъдат посочени като изключително рядък потенциален страничен ефект“, посочват от „АстраЗенека“.
Като цяло и двата прегледа потвърдиха, че ваксината предлага високо ниво на защита срещу заболяване от COVID-19 в целия спектър на тежест на протичане и че ползите от ваксината продължават да надвишават рисковете, допълват от там.
„В допълнение Световната здравна организация (СЗО) заяви, че въз основа на текущата информация причинно-следствената връзка се счита за вероятна, но не е потвърдена, добавяйки, че са необходими допълнителни специализирани проучвания, за да се разбере напълно потенциалната връзка между ваксинацията и възможните рискови фактори. СЗО отбеляза още, че макар и да са повод за загриженост, оценяваните събития са много редки, като се съобщава за нисък брой сред почти 200 милиона лица, получили ваксината на „АстраЗенека“ по целия свят“, се казва в позицията на компанията.