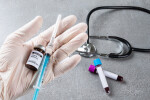
Европейската агенция по лекарствата стартира проучване за ползите и рисковете при китайската ваксината „Синовак“, за да реши дали да я разреши за употреба в Европейския съюз.
Решението на комисията по лекарства за хуманна употреба към агенцията "да започне проучване се базира на предварителни резултати от лабораторни изследвания (неклинични данни) и от клинични изследвания", обясни в комюнике европейският регулатор със седалище в Амстердам.
Във ваксината на "Синовак" е използван класическият метод с инактивиран вирус, подпомагащ организма на ваксинирания да изработва антитела срещу причинителя на болестта.
Изследванията показват, че ваксината задейства изработването на антитела, насочени срещу вируса, който предизвиква COVID-19, и способни да подпомогнат защитата срещу тази болест, добавя агенцията.
Тя ще продължи процедурата, докато получи достатъчно данни, за да може лабораторията да подаде официално искане за разрешение да пусне продукта си на пазара.
Европейската агенция по лекарствата "не може да предвиди общ график, но разглеждането на евентуалното искане се очаква да трае по-малко от обичайното с оглед работата, извършена по време на проучването", се казва в комюникето.
През февруари ваксината на "Синовак" бе разрешена в Китай. Разрешена е също в Чили, Бразилия, Филипините, Украйна и Турция.
Европейският регулатор започна оценка за разрешаване и на ваксината на "Пфайзер"/"Бионтех" за младежи над 12 годишна възраст. В момента този препарат е одобрен за употреба за хора над 16 години.
Очаква се Американската агенция по храните и лекарствата също да я разреши за младежи в началото на следващата седмица.