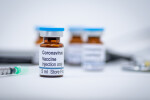
Фармацевтичната компания „Модерна“ е кандидатствала за спешно одобрение на ваксината си срещу COVID-19 в Американската агенция по храните и лекарствата.
Според производителя пълните резултати от последната фаза на изследванията са показали 94,1% ефективност на ваксината, без сериозни притеснения за безопасността й.
Компанията възнамерява да кандидатства за одобрение и в Европа.
Американският регулатор ще разгледа молбата за одобрение на заседание на 17 декември. Американската администрация отпусна на „Модерна“ 486 млн. долара за разработването на ваксина срещу новия коронавирус. Ако ваксината бъде одобрена, тя ще може да се поставя на американци още от 21 декември нататък.
Според данните от компанията проучването, в което са взели участие 30 000 доброволци, покрива всички критерии за одобрение на медикамента. Важен детайл е, че препаратът на „Модерна“ предотвратява на 100% тежко боледуване от коронавирус.
Компанията твърди, че до края на декември може да произведе 20 млн. дози и между 500 млн. и 1 млрд. през 2021 г. Както при останалите ваксини за COVID-19 и тази е с два приема, което означава, че 20 млн. дози ще стигнат за 10 млн. души.
„Модерна“ е втората компания, която кандидатства за спешно одобрение на ваксината си. „Пфайзер“ подаде документи за същата процедура още на 20 ноември.
И при двете ваксини, първите дози ще бъдат инжектирани на определени групи – медицински персонал, служители на първа линия и хора от рисковите групи.
Повече от 70 са ваксините срещу новия коронавирус, които се разработват по цял свят. От тях 11, включително тези на „Модерна“ и „Пфайзер“ са в етап на мащабно клинично тестване.